About Antibody

2013
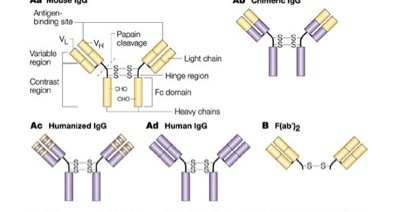
แอนติบอดี (antibody) เป็นสารชีวโมเลกุลที่มีคุณประโยชน์ต่อการค้นคว้าและวิจัยทางด้านวิทยาศาสตร์ชีวภาพแขนงต่างๆ อย่างยิ่ง [1-3] นอกจากนั้นแล้ว antibody ยังมีประโยชน์ในการใช้เป็นสารตรวจสอบที่มีความแม่นยำสูง [4-10] รวมทั้งเป็นยาที่มีประสิทธิภาพสูงในการรักษาโรค [3, 10-12] ทั้งนี้เพราะ antibody สามารถจับกับเป้าหมาย หรือ แอนติเจน (antigen) ได้อย่างจำเพาะเจาะจง ซึ่งคุณสมบัตินี้เป็นผลงานของธรรมชาติที่ผ่านการวิวัฒนาการมาหลายร้อยล้านปี หน้าที่หลักของ antibody ในสิ่งมีชีวิตคือการเป็นส่วนหนึ่งของระบบภูมิคุ้มกันของร่างกาย [13] ซึ่งจากความเข้าใจในกลไกการทำงานของธรรมชาติในด้านนี้เอง จึงทำให้มนุษย์สามารถประยุกต์ใช้ความรู้นี้ ในการสร้างเป็นเทคโนโลยีการผลิต antibody ชนิดต่างๆ ซึ่งมีประโยชน์ทั้งในการศึกษาวิจัย และการตรวจวินิจฉัย รวมทั้งการรักษาโรค ในชั้นต้น antibody สามารถผลิตได้จากการฉีดสาร antigen เข้าไปในสัตว์มีกระดูกสันหลังชนิดต่างๆ เช่น กระต่าย ม้า โค แพะ แล้วสกัด เอา antibody ซึ่งมีลักษณะเป็นโพลีโคลนอล (polyclonal antibody) ออกมาจากซีรั่ม [2] ต่อมาได้มีการพัฒนาวิธีการผลิต antibody อีกชนิดหนึ่งคือ monoclonal antibody [14] วิธีการทั่วไปที่ใช้ในการผลิต monoclonal antibody นั้น ทำได้โดยการฉีดแอนติเจน (antigen) เข้าไปในหนูเพื่อให้สร้างภูมิคุ้มกันต่อ antigen ชนิดนั้นๆ จากนั้นจึงใช้เทคนิคการสร้างเซลล์ผสม (hybridoma technology) เพื่อผลิตเป็น monoclonal antibody ชนิดต่างๆกัน เซลล์ผสมที่ถูกสร้างขึ้นให้มีความสามารถในการผลิต monoclonal antibody นั้น สามารถเก็บรักษาไว้ให้เป็นแหล่งผลิต monoclonal antibody ที่มีเอกลักษณ์ในความจำเพาะเจาะจง (unique specificity) ได้ตลอดไป การผลิต monoclonal antibody ชนิดหนึ่งๆ แต่ละครั้งนั้นต้องใช้เวลานาน ประมาณ ๔-๕ เดือนขึ้นไป และ การลงทุนสูง ทั้งยังต้องการบุคลากรที่มีความชำนาญสูง รวมทั้งยังต้องเกี่ยวข้องกับสัตว์ทดลองคือหนูอีกด้วย นอกจากการผลิต monoclonal antibody โดยวิธีการดั้งเดิมจะมีความยุ่งยากและค่าใช้จ่ายที่สูงแล้ว ยังมีข้อจำกัดที่เกิดจากเทคโนโลยีนี้หลายอย่างเช่น ข้อจำกัดเกี่ยวกับชนิดของ antigen ที่จะใช้ เพราะต้องเป็น antigen ที่ไม่เป็นพิษต่อหนูทดลอง และต้องไม่เป็น antigen ที่คล้ายกับ antigen ของหนู เช่น antigen ซึ่งเป็นโปรตีนที่อยู่ในขั้นต้นของลำดับการวิวัฒนาการ (conserved antigens) หรือใช้ได้เฉพาะกับ antigen ที่มีความสามารถในการกระตุ้นระบบภูมิคุ้มกัน (immunogenecity) ได้เท่านั้น รวมทั้งผลที่ได้จากการกระตุ้นหนูทดลองยังมีความแปรปรวนสูงขึ้นกับสุขภาพของหนูแต่ละตัว ข้อจำกัดที่สำคัญอีกประการหนึ่งก็คือจำนวนชนิดของ antigen ที่จะใช้ในการสร้าง monoclonal antibody เพราะ โดยปกติการผลิต monoclonal antibody ต่อ antigen แต่ละชนิดมักต้องใช้หนูทดลอง ๓-๕ ตัวขึ้นไป ในยุคปัจจุบันซึ่งเป็นยุคหลังการค้นพบลำดับ ยีโนมมนุษย์และสิ่งมีชีวิตอีกหลายชนิด (post-genomic era) ความสำคัญในการศึกษาวิจัยจึงมุ่งไปสู่การศึกษาการทำงานของยีโนม หรือโปรตีน (functional genomics หรือ proteomics) [15-24] ซึ่งการวิจัยเหล่านี้จำเป็นต้องเกี่ยวกับโปรตีนจำนวนมาก การสร้าง monoclonal antibody จำนวนมากเพื่อใช้ในการศึกษาการทำงานของโปรตีนหลายชนิดพร้อมๆกันโดยวิธีการที่ใช้อยู่ในปัจจุบัน จึงเป็นไปไม่ได้ หรือต้องใช้ค่าใช้จ่ายที่สูงมาก
การประยุกต์ใช้ monoclonal antibody อีกประการหนึ่งที่กำลังได้รับความสนใจอยู่มากในปัจจุบันนี้ ได้แก่การนำ monoclonal antibody ที่ผลิตได้จากหนูไปปรับปรุงให้มีคุณสมบัติเหมือนของมนุษย์ (humanization) [25, 26] เพื่อให้สามารถใช้ในการบำบัดโรคต่างๆ (human therapy) ปัจจุบันมี monoclonal antibody ที่มีข้อบ่งใช้ในการรักษาโรคมะเร็งหลายประเภทออกจำหน่ายแล้ว [27, 28] การประยุกต์ใช้ monoclonal antibody เพื่อใช้ในการรักษาโรคนี้นับวันจะมีความสำคัญและได้รับความนิยมเพิ่มมากขึ้น ดังนั้นจึงเป็นการดีที่จะใช้เทคโนโลยีอื่นในการผลิต monoclonal antibody ที่ไม่ยุ่งยากและรวดเร็วกว่าวิธีการ hybridoma ที่ใช้อยู่ในปัจจุบัน
เอกสารอ้างอิง
[1] Harlow, E., Lane, D., Using Antibodies : A Laboratory Manual : Portable Protocol, Cold Spring Harbor Laboratory Press 1998.
[2] Howard, G. C., Kaser, M. R. (Eds.), Making and Using Antibodies: A Practical handbook, CRC 2006.
[3] Winter, G., Milstein, C., Man-made antibodies. Nature 1991, 349, 293-299.
[4] Borrebaeck, C. A., Antibodies in diagnostics - from immunoassays to protein chips. Immunol Today 2000, 21, 379-382.
[5] Buscombe, J. R., The future of infection imaging. Q J Nucl Med Mol Imaging 2006, 50, 99-103.
[6] Coe Clough, N. E., Hauer, P. J., Using polyclonal and monoclonal antibodies in regulatory testing of biological products. ILAR J 2005, 46, 300-306.
[7] Laurino, J. P., Shi, Q., Ge, J., Monoclonal antibodies, antigens and molecular diagnostics: a practical overview. Ann Clin Lab Sci 1999, 29, 158-166.
[8] Moulds, M. K., Review: monoclonal reagents and detection of unusual or rare phenotypes or antibodies. Immunohematol 2006, 22, 52-63.
[9] Van de Wiele, C., Revets, H., Mertens, N., Radioimmunoimaging. Advances and prospects. Q J Nucl Med Mol Imaging 2004, 48, 317-325.
[10] Waldmann, T. A., Monoclonal antibodies in diagnosis and therapy. Science 1991, 252, 1657-1662.
[11] Blattman, J. N., Greenberg, P. D., Cancer immunotherapy: a treatment for the masses. Science 2004, 305, 200-205.
[12] Dubel, S., Handbook of Therapeutic Antibody, Wiley-VCH 2007.
[13] Janeway, A. C., Travers, P., Walport, M., Shlomshik, J. M. , Immunobiology : , Garland Publisher, New York 2008.
[14] Albitar, M. (Ed.), Monoclonal Antibodies: Methods and Protocols Humana Press 2007.
[15] Barry, R., Soloviev, M., Quantitative protein profiling using antibody arrays. Proteomics 2004, 4, 3717-3726.
[16] Borrebaeck, C. A., Antibody microarray-based oncoproteomics. Expert Opin Biol Ther 2006, 6, 833-838.
[17] Borrebaeck, C. A., Wingren, C., High-throughput proteomics using antibody microarrays: an update. Expert Rev Mol Diagn 2007, 7, 673-686.
[18] Borrebaeck, C. A. K., Antibodies in diagnostics - from immunoassays to protein chips. Immunology Today 2000, 21, 379-382.
[19] Bradbury, A., Velappan, N., Verzillo, V., Ovecka, M., Chasteen, L., Sblattero, D., Marzari, R., Lou, J., Siegel, R., Pavlik, P. , Antibodies in proteomics I: generating antibodies. Trends in Biotechnology 2003a, 21, 275-281
[20] Bradbury, A., Velappan, N., Verzillo, V., Ovecka, M., Chasteen, L., Sblattero, D., Marzari, R., Lou, J., Siegel, R., Pavlik, P. , Antibodies in proteomics II: screening, high-throughput characterization and downstream applications. Trends in Biotechnology 2003b, 21, 312-317.
[21] Elrick, M. M., Walgren, J. L., Mitchell, M. D., Thompson, D. C., Proteomics: recent applications and new technologies. Basic Clin Pharmacol Toxicol 2006, 98, 432-441.
[22] Glokler, J., Angenendt, P., Protein and antibody microarray technology. J Chromatogr B Analyt Technol Biomed Life Sci 2003, 797, 229-240.
[23] Kopf, E., Zharhary, D., Antibody arrays--an emerging tool in cancer proteomics. Int J Biochem Cell Biol 2007, 39, 1305-1317.
[24] Kusnezow, W., Syagailo, Y. V., Goychuk, I., Hoheisel, J. D., Wild, D. G., Antibody microarrays: the crucial impact of mass transport on assay kinetics and sensitivity. Expert Rev Mol Diagn 2006, 6, 111-124.
[25] Almagro, J. C., Fransson, J., Humanization of antibodies. Front Biosci 2008, 13, 1619-1633.
[26] Clark, M., Antibody humanization: a case of the 'Emperor's new clothes'? Immunol Today 2000, 21, 397-402.
[27] Khandare, J. J., Minko, T., Antibodies and peptides in cancer therapy. Crit Rev Ther Drug Carrier Syst 2006, 23, 401-435.
[28] Schrama, D., Reisfeld, R. A., Becker, J. C., Antibody targeted drugs as cancer therapeutics. Nat Rev Drug Discov 2006, 5, 147-159.
นำเรื่อง แอนติบอดี
9/13/2556
Links to Useful Sites
The Nobel Prize in Immunology
http://www.nobelprize.org/nobel_prizes/medicine/immune_responses.html
The Nobel Prize in Physiology or Medicine 2011
http://www.nobelprize.org/nobel_prizes/medicine/laureates/2011/
The Immune System Game
hhttp://www.nobelprize.org/educational/medicine/immunity/
The Immune Response Game
http://www.nobelprize.org/educational/medicine/immuneresponses/
