Monoclonal Antibody

2013
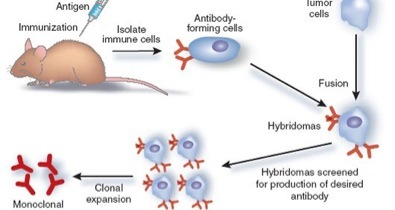
โมโนโคลนอล แอนติบอดี (monoclonal antibody) [1-3] ไม่ใช่สารที่เกิดจากธรรมชาติ แต่เกิดจากการที่มนุษย์คิดค้นวิธีการสร้างขึ้นด้วยเทคโนโลยีทางอณูชีววิทยาในปี พ.ศ. ๒๕๑๘ วิธีการทั่วไปที่ใช้ในการผลิต monoclonal antibody นั้น ทำได้โดยการฉีด antigen เข้าไปในหนูเพื่อให้สร้างภูมิคุ้มกันต่อ antigen ชนิดนั้นๆ จากนั้นจึงใช้เทคนิคการสร้างเซลล์ผสม (hybridoma technology) ระหว่าง B lymphocyte และ myeloma cell หรือเซลล์มะเร็งเม็ดเลือดขาว เพื่อผลิตให้ได้เป็น monoclonal antibody ชนิดต่างๆกัน [2] ดังรูปที่ ๑ ซึ่งแสดงขั้นตอน การผลิต monoclonal antibody ที่เร่ิมจากการกระตุ้นระบบภูมิคุ้มกันของหนูด้วย antigen ในภาพนี้คือ antigen X จากนั้นทำการสกัด B lymphocyte ที่ทำหน้าที่สร้าง antibody ออกมา B lymphocyte นี้ไม่สามารถเลี้ยงต่อได้ จึงต้องนำไปเชื่อมรวมกับ tumor cell ของ B lymphocyte ที่มีความสามาถในการโตบนจานเลี้ยงเซลได้ไม่จำกัด (immortal) เพื่อสร้างเป็น hybridomas ที่มีความสามารถในการหลั่ง monoclonal antibody ที่ต้องการ หลังจากที่ได้ทำการเชื่อมรวมเซลแล้วจะต้องทำการคัดแยกเอาเฉพาะ hybridomas โดยการเลี้ยงในอาหารที่มีสารยับยั้งกระบวนการสังเคราะห์ nucleotides (aminopterin) แบบปกติ ดังนั้นเซลที่จะเจริญต่อไปได้ต้องมีกระบวนการสังเคราะห์ลัด (bypass pathway) ซึ่งกระบวนการนี้มีเฉพาะใน B lymphocyte ที่ปกติเท่านั้น ทำให้ B lymphocyte ที่เป็นtumor โตไม่ได้ หลังจากที่คัดเลือก hybridomas ได้แล้ว จะต้องนำไปคัดแยกหาโคลนเดี่ยวที่มีความสามารถในการสร้าง antibody ต่อ antigen X ที่ต้องการได้ ขั้นตอนทั้งหมดใช้เวลานานหลานเดือน ค่าใช้จ่ายสูง และต้องการบุคคลากรที่มีความชำนาญสูง โคลนของ hybridoma ที่สามารถผลิต antibody ที่ต้องการนี้สามารถเก็บไว้ใช้ได้ตลอดไป
เซลล์ผสมที่ถูกสร้างขึ้นให้มีความสามารถในการผลิต monoclonal antibody นั้น สามารถเก็บรักษาไว้ให้เป็นแหล่งผลิต monoclonal antibody ได้ตลอดไป การผลิต monoclonal antibody ชนิดหนึ่งๆ แต่ละครั้งนั้นต้องใช้เวลานาน (๔-๕ เดือนขึ้นไป) และ การลงทุนเป็นจำนวนสูง นอกจากนั้นแล้วยังต้องการบุคลากรที่มีความชำนาญสูง รวมทั้งยังต้องเกี่ยวข้องกับสัตว์ทดลองคือ หนู อีกด้วย [1]
ดังนั้นจึงเห็นได้ว่าขบวนการการผลิต monoclonal antibody ที่ใช้กันอยู่ในปัจจุบันนั้นค่อนข้างยุ่งยาก บางครั้งนักวิจัยไม่มีเวลาหรือบุคลากรเพียงพอ จึงต้องสั่งทำจากต่างประเทศซึ่งมีราคาสูง และยังมี อุปสรรคที่สำคัญอีกประการหนึ่งของการใช้เทคโนโลยี hybridoma ในการผลิต monoclonal antibody ก็คือ hybridoma cell ไม่เสถียร ทำให้สามารถสูญเสียความสามารถในการผลิต monoclonal antibody ได้ อีกทั้งในขั้นตอนการผลิต monoclonal antibody ให้ได้เป็นจำนวนมาก (large scale) เพื่อการนำไปใช้ต่อนั้นก็มีความยุ่งยากและต้องใช้เครื่องมือราคาแพงเช่นกัน วิธีการที่นิยมใช้ในการผลิต monoclonal antibody ให้ได้เป็นจำนวนมากนั้นมี ๒ วิธีคือ การนำ hybridomas ไปเลี้ยงในลักษณะที่เป็นมะเร็งในช่องท้องของหนู (ascites tumor) แล้วสกัดเอา ascites fluid ที่มี monoclonal antibody ออกมา วิธีนี้เป็นที่นิยมเพราะสามารถผลิตได้ monoclonal antibody ในปริมาณสูงกว่าการเลี้ยงในห้องทดลองถึง ๑,๐๐๐ – ๑๐,๐๐๐ เท่า แต่เป็นวิธีการที่สร้างความเจ็บปวดและทรมานให้กับหนูทดลอง นอกจากนั้นแล้ว monoclonal antibody ที่เตรียมได้ยังปนเปื้อนด้วย immunoglobulin ของหนู ไวรัส หรือสาร cytokine อื่นๆจากหนูซึ่งอาจไม่เป็นผลดีต่อการประยุกต์ใช้ต่อไป [1] วิธีการอีกวิธีหนึ่งในการผลิต monoclonal antibody เป็นจำนวนมากคือการเลี้ยงใน bioreactor ชนิดต่างๆได้แก่ standard static หรือ agitated suspension cell cultures, membrane-based หรือ matrix-based culture systems, และ high cell-density bioreactors [4, 5] แต่ข้อจำกัดของวิธีการเหล่านี้คือเป็นเทคโนโลยีที่ต้องใช้เครื่องมือที่มีราคาสูงมากรวมทั้งอาหารและสารเคมีที่ใช้ในการเลี้ยงเซลล์ก็มีราคาสูงมากเช่นกัน
นอกจากการผลิตโมโนโคลนอล antibody โดยวิธีการดั้งเดิมนั้นจะมีความยุ่งยากและค่าใช้จ่ายที่สูงแล้ว ยังมีข้อจำกัดที่เกิดจากเทคโนโลยีนี้หลายอย่างเช่น ข้อจำกัดในชนิดของ antigen ที่จะใช้ เพราะต้องเป็น antigen ที่ไม่เป็นพิษต่อหนูทดลอง นอกจากนั้นแล้วยังต้องไม่เป็น antigen ที่คล้ายกับ antigen ของหนู เช่น antigen ซึ่งเป็นโปรตีนที่อยู่ในขั้นต้นของลำดับการวิวัฒนาการ (conserved antigens) หรือใช้ได้เฉพาะกับ antigen ที่มีความสามารถในการกระตุ้นระบบภูมิคุ้มกันของหนู (immunogenicity) ได้เท่านั้น นอกจากนั้นแล้วผลที่ได้จากการกระตุ้นหนูทดลองยังมีความแปรปรวนสูงขึ้นกับสุขภาพของหนูแต่ละตัว ข้อจำกัดที่สำคัญอีกประการหนึ่งก็คือจำนวนชนิดของ antigen ที่จะใช้ในการสร้าง monoclonal antibody โดยปกติการผลิต monoclonal antibody ต่อ antigen แต่ละชนิดมักต้องใช้หนูทดลอง ๓-๕ ตัวขึ้นไป ในยุคปัจจุบันซึ่งเป็นยุคหลังการค้นพบลำดับยีโนม (post-genomic era) ของมนุษย์ และสิ่งมีชีวิตอีกหลายชนิด ความสำคัญในการศึกษาวิจัยจึงมุ่งไปสู่การศึกษาการทำงานของยีโนม หรือโปรตีน (functional genomics หรือ proteomics) ซึ่งการวิจัยเหล่านี้จำเป็นต้องเกี่ยวกับโปรตีนจำนวนมหาศาล (high-througput) การสร้าง monoclonal antibody จำนวนมากเพื่อใช้ในการศึกษาการทำงานของโปรตีนเหล่านี้โดยวิธีการที่ใช้อยู่ในปัจจุบันจึงเป็นไปไม่ได้ หรือต้องการค่าใช้จ่ายที่สูงมาก จึงมีความจำเป็นต้องใช้เทคโนโลยีอื่นในการผลิตโมโนโคลนอลแอนติบอดี เพื่อการวิเคราะห์ในระดับ high-througput เหล่านี้ [6-8]
การประยุกต์ใช้ monoclonal antibody ที่กำลังได้รับความสนใจอยู่มากอีกประการหนึ่งในปัจจุบันนี้ ได้แก่การนำ monoclonal antibody ที่ผลิตได้จากหนูไปปรับปรุงให้มีคุณสมบัติเป็นเหมือนของมนุษย์ (humanization) เพื่อให้สามารถใช้ในการบำบัดโรคต่างๆ (human therapy) [9-11] ปัจจุบันมี monoclonal antibody ที่มีข้อบ่งใช้ในการรักษาโรคต่างๆ เช่นมะเร็งเต้านมขั้นสุดท้ายออกจำหน่ายแล้ว [12] การประยุกต์ใช้ monoclonal antibody เพื่อใช้ในการรักษาโรคนี้นับวันจะมีความสำคัญและได้รับความนิยมเพิ่มมากขึ้น ดังนั้นจึงเป็นการดีที่จะใช้เทคโนโลยีอื่นในการผลิต monoclonal antibody ที่ไม่ยุ่งยาก และรวดเร็วกว่าวิธีการ hybridoma ที่ใช้อยู่ในปัจจุบัน
เอกสารอ้างอิง
[1] Albitar, M. (Ed.), Monoclonal Antibodies: Methods and Protocols Humana Press 2007.
[2] Laurino, J. P., Shi, Q., Ge, J., Monoclonal antibodies, antigens and molecular diagnostics: a practical overview. Ann Clin Lab Sci 1999, 29, 158-166.
[3] Lipman, N. S., Jackson, L. R., Trudel, L. J., Weis-Garcia, F., Monoclonal versus polyclonal antibodies: distinguishing characteristics, applications, and information resources. ILAR J 2005, 46, 258-268.
[4] Birch, J. R., Racher, A. J., Antibody production. Adv Drug Deliv Rev 2006, 58, 671-685.
[5] Kelley, B., Very large scale monoclonal antibody purification: the case for conventional unit operations. Biotechnol Prog 2007, 23, 995-1008.
[6] Elrick, M. M., Walgren, J. L., Mitchell, M. D., Thompson, D. C., Proteomics: recent applications and new technologies. Basic Clin Pharmacol Toxicol 2006, 98, 432-441.
[7] Glokler, J., Angenendt, P., Protein and antibody microarray technology. J Chromatogr B Analyt Technol Biomed Life Sci 2003, 797, 229-240.
[8] Kusnezow, W., Hoheisel, J. D., Antibody microarrays: promises and problems. Biotechniques 2002, Suppl, 14-23.
[9] W., P., E. F. L. J., A., Mutarotation and actions of acids and bases, in the carbohydrates chemistry and biochemistry, in: W., P., Horton, D. (Eds.), Acadamic Press, New York 1972.
[10] Waldmann, T. A., Monoclonal antibodies in diagnosis and therapy. Science 1991, 252, 1657-1662.
[11] Winter, G., Milstein, C., Man-made antibodies. Nature 1991, 349, 293-299.
[12] Plosker, G. L., Keam, S. J., Trastuzumab: a review of its use in the management of HER2-positive metastatic and early-stage breast cancer. Drugs 2006, 66, 449-475.
โมโนโคลนอลแอนติบอดี
9/13/2556
